|  |
 PontusWallstedt / UgglansNO
PontusWallstedt / UgglansNO
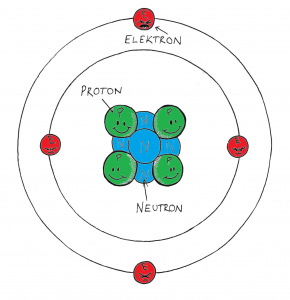
Atomen består av en kärna med protoner (positivt laddade) och neutroner (neutralt laddade). Runt atomkärnan finns elektroner (negativt laddade) i olika elektronskal. Antalet protoner bestämmer vilket grundämne det är. Elektronerna i det yttersta elektronskalet (valenselektroner) bestämmer grundämnets egenskaper.
Bild: Clker-Free-Vector-Images / Pixabay License
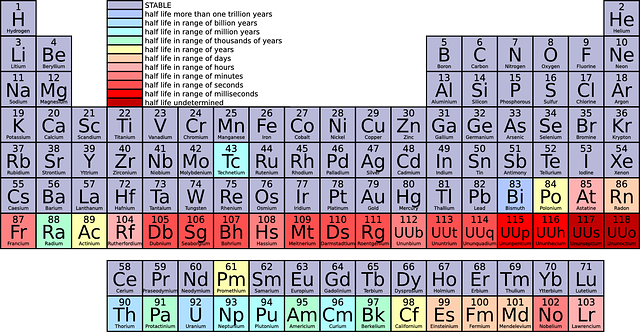
I det periodiska systemet finns alla grundämnen som är kända idag. Som grundämne, uppställt i periodiska systemet, har det alltid lika många elektroner som protoner. Ett grundämne är alltså oladdat. Grundämnen eftersträvar fullt yttre elektronskal. Därför ger/tar eller lånar de elektroner med andra atomer. Om en atom inte har lika många protoner (positiva laddningar) som elektroner (negativa laddningar) kallas den jon. En atom blir en positiv jon om den har förlorat elektroner och en negativ jon om den har tagit upp elektroner.

Bild: Oskar Uggla / UgglansNO
Elektronskal är de energinivåer som elektronerna färdas i. Skalen börjar namnges från atomkärnan med bokstaven K. K-skalet kan max innehålla två elektroner, L-skalet åtta. Det yttersta elektronskalet kan max innehålla åtta elektroner oavsett vilken bokstav det har (undantag om det är K-skalet).
Sammanfattning: Antalet protoner avgör vilket grundämne det är. Antalet elektroner bestämmer om grundämnet är en jon (laddat) eller oladdat. Antalet neutroner avgör vilken isotop av grundämnet det är. En isotop är en variant av ett grundämne. Alla grundämnen har isotoper. Isotoperna av ett grundämne får olika egenskaper. Framförallt avgör det om ämnet är radioaktivt eller inte.
Fördjupning:
- Film – Atomen (Andreas Sandqvist, 9.58, Svenska)
- Film – Atomens byggnad (Bertram Stenlund, Svenska, 5,04)
- Hemsida – Det periodiska systemet (naturvetenskap.org)
- Hemsida – Joner (naturvetenskap.org)
- Film – Atoms explained (Kurzgesagt, 4.58, Engelska)
- Film – Niels Bohr (Urplay, 18.00, svenska)
Uppgifter:
| Hela kursen: | Kursens begrepp: | Kursens test: |
| Atomfysik | Quizlet – Tabs | Deltest – Stortest |
Hjälp till att förbättra Ugglans NO! Har du hittat något fel, någon död/olämplig länk eller vill tipsa om någon intressant länk? Skriv en kommentar nedan!